理想気液混合物として、理想気体とファンデルワールス流体の混合物を取り上げ、 その相挙動を見てきました。 ここでは臨界温度の差が大きい 水素 H2- 水 H2O 混合系と ヘリウム He -キセノン Xe 混合系を取り上げ、 その相挙動を理想気液混合系と比較検討してみます。 水素、ヘリウムともにかつて「永久気体 permanent gas」と呼ばれたように、 通常の温度ではあくまで気体として振舞うことが期待され、 ここでは気体成分と呼ぶことにします。
水素 H2 の臨界パラメーターは、臨界温度 \(T_\mrm{C}\) = 33.1 K、臨界圧力 \(P_\mrm{C}\) = 1.3 MPa、臨界密度 \(\rho_\mrm{C}\) = 0.015 mol cm-3、 水 H2O の臨界パラメーターは、\(T_\mrm{C}\) = 647.1 K、\(P_\mrm{C}\) = 22.1 MPa、\(\rho_\mrm{C}\) = 0.018 mol cm-3 で、臨界温度、臨界圧力だけ取れば水素は水の 20 分の 1 ぐらい。 水素は気体成分と見なせ、 理想気液混合物の理想気体成分 X のように振舞うと思ってもよいでしょう。 ただし臨界密度は同程度で排除体積の効果は無視できず、 このことがどのように影響を及ぼすのか興味のあるところです。

|
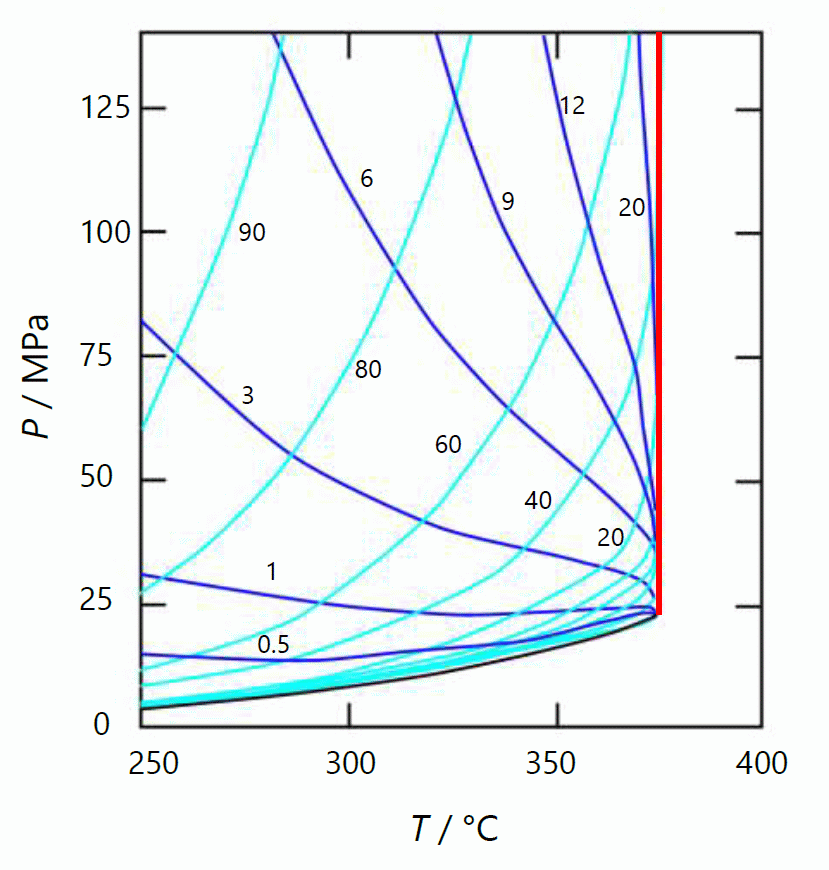
| 図 7-1. 水素 H2- 水 H2O 混合系の温度 \(P\) -圧力 \(T\) 面での等組成の相図。 赤い実線は臨界線 \(T_\mrm{C}\) 。 露点曲線(水色)、泡点曲線(青)に添えた数字は、 水素 H2 のモル百分率。 Seward らによる図を縮尺を変えて改変。 ぼくのトレースが下手くそで、少しガタついていますがご容赦のほど・・・ |
図 7-1 に示すのは、Seward らによって実験的に得られている 水素 H2- 水 H2O 混合系の \((P, T)\) 図です。 実験は 200 °C 付近から、440 °C、250 MPa までの高温・高圧領域について、 水素 H2 のモル分率 0.5 % から 90 % の混合比について行われています。 実験的には水素のモル分率 40 % 以上の混合比では泡点が検出できていませんが、 水素のモル分率 40 % までは露点・泡点の等組成線は舌状(?)に温度軸に沿って伸び、 臨界点で接合しています。 そして臨界温度は、 水素のモル分率が 20 % 程度まで 374 °C でほとんど一定で、 それ以上モル分率が増えると若干高くなりますが、モル分率 40 % でも 10 °C 上がって 383 °C 程度になるぐらいです。 一方臨界圧力は 22.1 MPa からモル分率 20 % で 69 MPa、40 % では 300 MPa と、 大きく増加しています。 露点曲線と泡点(沸点)曲線は臨界点で接合しますが、 実験的に得られている温度・圧力範囲では、 臨界点はほぼ圧力軸との接点、温度極大のところになります (臨界点が \((P, T) \)面の等組成線の極大・極小になる熱力学的な必然性はありません)。
図 7-1 は、大まかには理想気液混合物の相挙動と似かよっているように見えます。 けれども少し仔細に見てみると、 特に泡点の挙動に違いが認められます。
水素 H2- 水 H2O 混合系の臨界温度が水素の組成比にほとんど依存しないのは (モル分率 0.4 までのことではありますが)、 理想気液混合物の挙動と合致するところです。 一方臨界圧力についていうと、 水素の組成比とともに増加するのはよいのですが、 増加量は理想気液混合物から予想されるよりはるかに大きくなります。 理想気液混合物では、臨界圧力の理想気体成分のモル分率 \(x\) に対する依存性は次のように表されます:
\begin{equation} P_\mrm{C}(x) = P_\mrm{C}^{\star} + \frac{x}{1 - x} \rho^\star_\mrm{C} T_\mrm{C} = \frac{1}{27} + \frac{x}{1 - x} \frac{8}{81} \label{eq:mix_pc} \end{equation}
理想気液混合物の臨界圧力は、 理想気体成分 X のモル分率が 0.2 で純粋なファンデルワールス流体成分の臨界圧力の 1.67 倍、 0.4 で 2.78 倍になります。 一方、水素 H2- 水 H2O 混合系では、 水素のモル分率 0.2 で 3.1 倍、0.4 で 14 倍と、 臨界圧力は理想気液混合物に比して急速に大きくなっていきます。
臨界圧力が高くなるのと同様、 水素 H2- 水 H2O 混合系では、 臨界点から温度を下げていった時の泡点の圧力の上昇の度合いは、 理想気液混合物に比してはるかに大きくなり、 理想気液混合物では見られた泡点圧力の極大が認めがたくなります。 実際 \((P, T)\) 面の等組成線で、 水素のモル分率が 0.01 では泡点曲線の極大が確認できますが、 0.03 ではもはや(実験の範囲では)泡点曲線の極大は認められません。 またモル分率 0.005 の段階で温度の低下にともなう泡点圧力の低下は 300 K 付近で認めがたくなり、 理想気液混合物で見られた人だま型のループは(あったとしても)急速に消失していくようです。
|
|
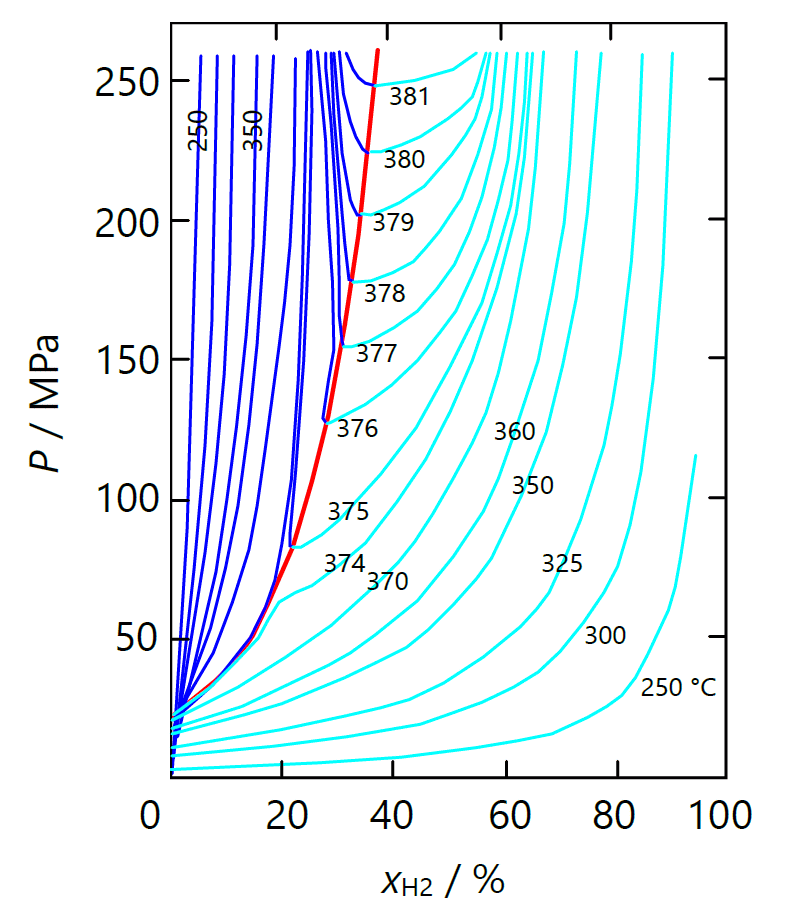
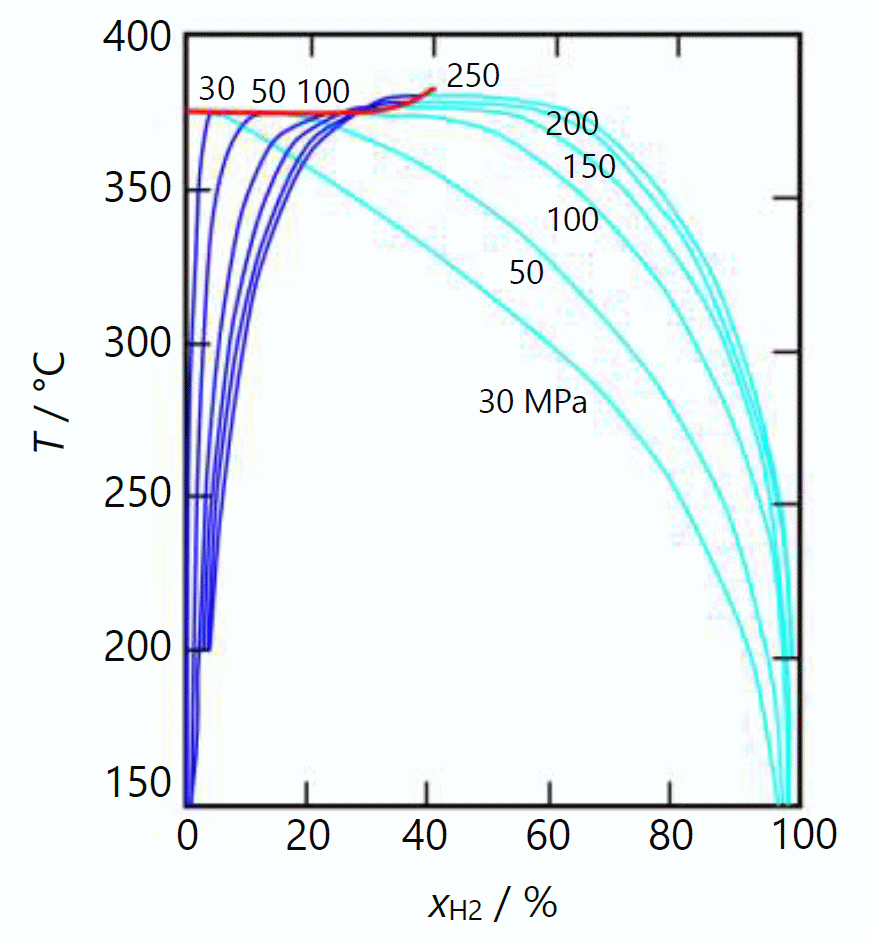
| 図 7-2. 水素 H2- 水 H2O 混合系の圧力 \(P\)-水素モル百分率 \(x_\mrm{H_2}\) 面での等温線。 赤い実線は臨界線 \(P_\mrm{C}\) 。 露点曲線(水色)、泡点曲線(青)に添えた数字は、 温度 \(T / {}^\circ \mrm{C}\)。 Seward らによる図を改変。 トレースが下手くそでガタついています。 | 図 7-3. 水素 H2- 水 H2O 混合系の温度 \(T\)-水素モル百分率 \(x_\mrm{H_2}\) 面での等圧線。 赤い実線は臨界線 \(T_\mrm{C}\) 。 露点曲線(水色)、泡点曲線(青)に添えた数字は、 圧力 \(P / \mrm{MPa}\)。 Seward らによる図を改変。 トレースが下手くそで、いささかガタついています。 |
理想気液混合物との差異は泡点(沸点)に顕著に現れているわけですが、 横軸にモル分率を取った等圧線図、等温線図で見ると、 より事態は明瞭です。 図 7-2 には水素 H2- 水 H2O 混合系の \((P, x)\) 面での露点・泡点の等温線を示しました (原図の横軸を理想気液混合系の図に合わせるように変更しています)。 露点曲線は水素のモル分率の増加とともに単調に増加し、 温度が高いほど露点圧力(凝縮圧)は高くなり、 臨界線に漸近していきます。 定性的には露点曲線の挙動は理想気液混合物の挙動と似かよって見えます。 泡点曲線は水素のモル分率の増加とともに増加し、 温度の上昇とともに右にシフトしていきます。 この挙動自体は理想気液混合物の泡点と似かよっていますが、 水素含有率の依存性が非常に大きく、また理想気液混合物の泡点曲線の温度依存性より単調な挙動になっています。
理想気液混合物との類似点、相違点は、 図 7-3 の \((T, x)\) 面での等圧線でみた方が明瞭かもしれません (原図の横軸を変更しています)。 水素 H2- 水 H2O 混合系の露点曲線の挙動は、 理想気液混合系の露点曲線と似かよっていて、 水素モル分率の増加にともない、等圧線は臨界温度から低温側に減少していきます。 また圧力増加にともない、等圧線は水素モル分率の高い側にシフトしていきます。 水素 H2- 水 H2O 混合系の沸点曲線は、 臨界温度から温度を下げていくと水素モル分率は概ね単調に減少していき、 理想気液混合系の泡点曲線で見られた水素モル分率の極小は、 圧力が 25 MPa 以下、水素モル分率 0.01 程度でようやく見られるにすぎません。 そのため図 7-3 では 理想気液混合系でみられた等圧線のループは 泡点曲線の途中で途切れた格好になっています。
ここで紹介した水素 H2- 水 H2O 混合系の実験は Seward と Frank によるものです。 原報を一読されることとをお薦めしますが、 実験は水素と水を詰めた容器の温度を 450 °C まで上げた後、ゆっくり下げる形で行われました。 目視観測とともに、圧力変化の異常を検知することで相変化をモニターしています。 過酷な条件の実験で、 時として圧力センサーが水素脆性の影響で破裂したりしたようです。 高温高圧の水素が噴出してくるかもしれない中、 水素と水の仕込み量を変えては、圧力容器が冷えていくまで 3 時間くらい付き合うという、 ちょっと引いてしまいそうな実験です。 けれども Frank のグループは 200 MPa、450 °C での水中のメタンの酸素による炎を実現するなど、 強心臓の持ち主たちぞろいのようです・・・。
|
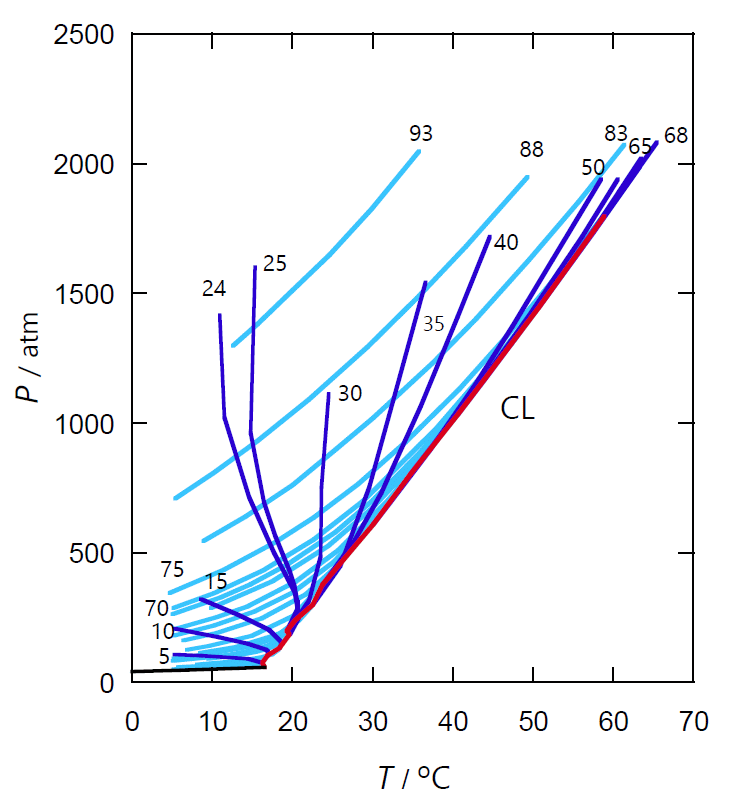
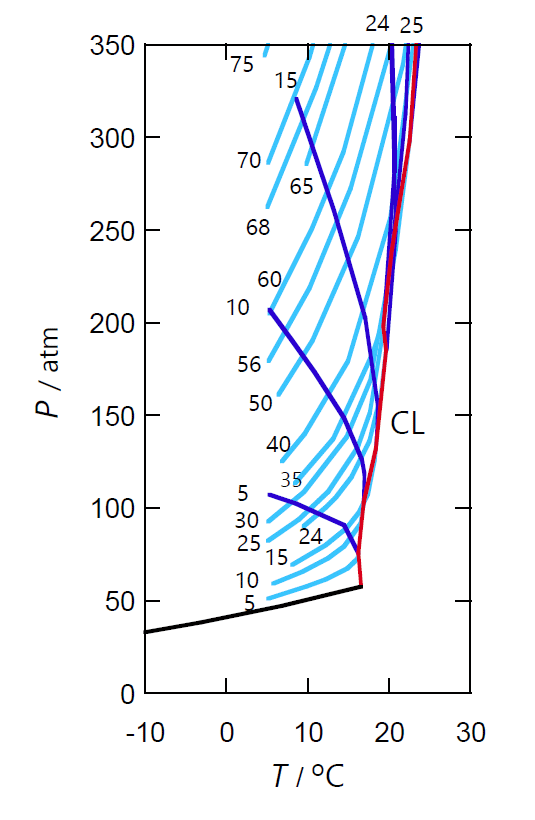
| 図 7-4a. ヘリウム He -キセノン Xe 混合物の \((P, T) \)面の等組成線 (1 atm = 0.101325 MPa。de Swaan Arons たちの図を改変)。 露点曲線(水色)、泡点曲線(青)に添えた数字は、 ヘリウム He のモル百分率。 図中、赤線は臨界線です。 |
前節でみた水素 H2- 水 H2O 混合系は、 水というしばしば異常扱いされる物質を扱っていました。 では単原子分子からなる、希ガスの混合物ではどうなるでしょうか? ヘリウム He の臨界パラメーターは、\(T_\mrm{C}\) = 5.2 K、\(P_\mrm{C}\) = 0.23 MPa、\(\rho_\mrm{C}\) = 0.018 mol cm-3、 キセノン Xe の臨界パラメーターは、\(T_\mrm{C}\) = 289.7 K、\(P_\mrm{C}\) = 5.8 MPa、\(\rho_\mrm{C}\) = 0.0085 mol cm-3 です。 ヘリウム He - キセノン Xe 混合系では、 臨界温度、臨界圧力だけ見れば水素 H2- 水 H2O 混合系と同様、 20 倍以上の違いがあり、ヘリウムはキセノンに対して気体成分として見ることができるでしょう。
図 7-4a に示すのは、de Swaan Arons たちによって得られた、 ヘリウム He - キセノン Xe 混合物の \((P, T) \) 図です (実験点を結んでいるので少しガタいています。 Pa ではなく気圧 atm 単位になっています)。
ヘリウム He - キセノン Xe 混合物の図 7-4a の相図は、 図 7-1 の水素 H2- 水 H2O 混合系とかなり異なっているように見えるかもしれません。 けれどもよく見ると似かよった挙動が見られます。 ヘリウム He のモル分率の増大とともに、 臨界圧力は急速に増大します。 一方臨界温度も増加しますが、臨界圧力に比べると増加の度合いははるかに小さいものに止まります (図中 2000 atm はキセノンの臨界圧力の 35 倍ですが、60 °C のちがいは臨界温度の 1/5 でしかありません)。 泡点曲線の挙動は単純ではありませんが、 露点曲線は温度とともに単調に増加し、 ヘリウム He のモル分率の増大とともに急速に増加していきます。 そして水素 H2- 水 H2O 混合系と同様、 ヘリウム He のモル分率が 30 % ぐらいまでは、 露点・泡点曲線が舌状に温度軸に沿って伸び、 臨界点で接合します。
|
| 図 7-4b. ヘリウム He -キセノン Xe 混合物の \((P, T) \)面の等組成線。 図 7-1 の水素 H2- 水 H2O 混合系の図に対応するように、 図 7-4a. を臨界パラメーターでスケールしたもの。 |
類似点を挙げてみましたが、図 7-1 と図 7-4a では、 やはり大きな差があるように見えます。 けれども水とキセノンの臨界温度・圧力で焼き直してみてみると、 事態の見え方は変わってきます。 先にヘリウム He - キセノン Xe 混合物で、 臨界圧力に比べると臨界温度の増加の度合いは、 臨界点に対する比率でみれば、はるかに小さいものになっていると述べました。 図 7-4b はヘリウム He - キセノン Xe 混合物の実験結果を、 水素 H2- 水 H2O 混合物の臨界パラメーターを用いて、 図 7-1 のスケールにおおよそ合わせたものです。 臨界温度・圧力でスケールし直してみると、 水素 H2- 水 H2O 混合物と ヘリウム He - キセノン Xe 混合物の相挙動が非常に似かよっていることに気づかされます。
両方の系を勘案してみると、 臨界温度・圧力が低く気体成分のモル分率が非常に小さい(0.02 程度以下)では、 現実系でも臨界点付近で理想気液混合物で見られるような人だま型のループの部分構造が認められます。 また水素 H2- 水 H2O 混合物を取ってみると、 常温付近の泡点は水素気体の溶解度に相当するわけですが、 0.1 MPa でモル分率 1.4 × 10-5 程度で 組成比がモル分率 10-5 ぐらいです。 非常に低モル分率では室温付近での泡点圧力は臨界圧力の 22 MPa から大きく減少し、 理想気液混合物で見られる人だま型のループになると考えてよいでしょう。 しかし気体成分のモル分率が増加するにつれ、泡点曲線は温度を下げるとともに増加するようになり、 ヘリウム He - キセノン Xe 混合物で端的にみられるように、 急速にループ構造は失われていくようです。
|
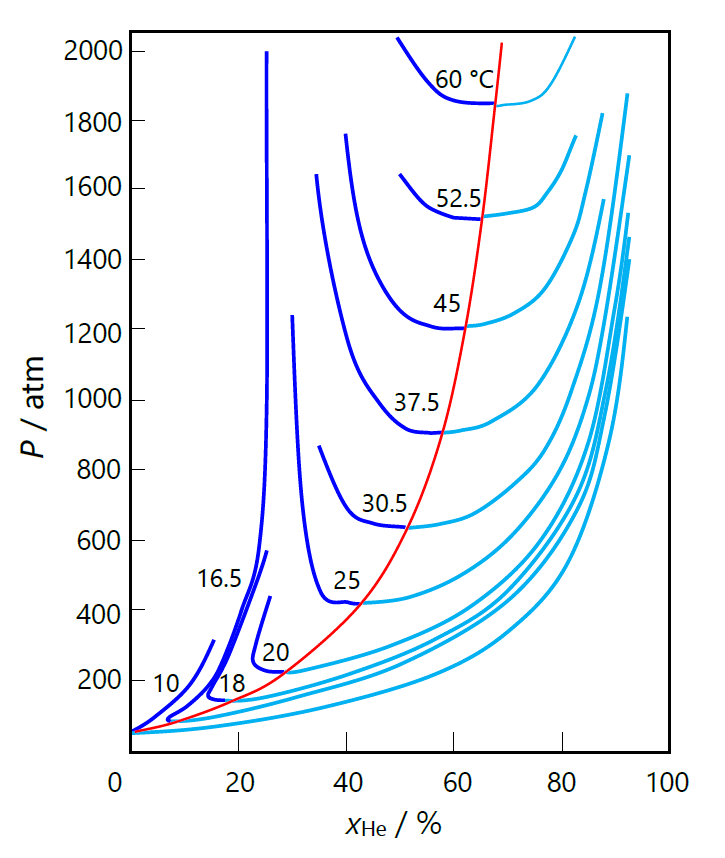
| 図 7-5. ヘリウム He -キセノン Xe 混合物の \((P, x) \)面の等温線。 (de Swaan Arons たちの図を改変)。 露点曲線は水色で、沸点曲線は青で示しています。 図中、赤線は臨界温度での等温線です。 |
図 7-5 に示すヘリウム He -キセノン Xe 混合物の \((P, x) \) 図でも同様に、 理想気液混合物と現実系との類似点と相違点が見て取れます。 気体成分(He)の組成比の増加とともに、 臨界圧力は急速に、臨界温度は少しずつ増加していきます。 ヘリウム He - キセノン Xe 混合物の露点の等温線は、 理想気液混合物と同様、気体成分(He)の組成比の増加とともに単調に増加していきます。 一方、泡点曲線は低温では理想気液混合物と同様に、 気体成分(He)の組成比の増加とともに増加していきますが、 温度が上がるとともに急速に減少に転じます。 そのため臨界点近くの形状が、最初は嘴(くちばし)型だったのが傾いた U 型(?)になり、さらには U 型 に変化していきます。
臨界温度・圧力の大きく異なる水素 H2- 水 H2O あるいはヘリウム He -キセノン Xe 混合物のような現実の気液混合系について、 気体成分の組成が小さい領域での挙動は、 理想気液混合物モデルでよく説明できるもののようです。 しかし気体成分の組成が大きくなるにしたがって、 理想気液混合物からの乖離は急速に大きくなっていきます。 この差を埋めるには、排除体積についての考慮が重要になってくるのでしょう。