2026.2
吉村洋介
0.物理化学・物性化学実験の準備ex
V. 凝固点降下
<概要>
純物質 S の液体にそれと固溶体を作らない物質 X を溶解させたとき、
S の凝固点は一般に低下する。
X の濃度が低ければ凝固点降下の大きさ ΔTf は、
X の S の単位質量あたりの物質量 m(質量モル濃度)に比例し、
その比例係数 Ef を凝固点降下定数と呼ぶ: ΔTf = Ef m。
X の S に対する質量比を w、X のモル質量を MX とすると
w = MXm なので、凝固点降下の大きさ ΔT
がわかれば X のモル質量は S の凝固点降下定数 Ef を用いて
\begin{equation}
M_\mrm{X} = w/m = \frac{w E_\mrm{f}}{\Delta T}
\label{eq:FpMW}
\end{equation}
で得ることができる。
S と X の分子量がおよそ 100 のオーダーであるとすると、
質量モル濃度が 0.1 mol/kg であれば X の物質量は S の 1/100 程度になり、
希薄溶液として扱え式 \eqref{eq:FpMW} が成立するであろう。
S としてシクロヘキサンを採用すると、0.1 mol/kg の凝固点降下度は 2 K 程度なので、
モル質量を 1/100 の精度で決めるには、凝固点降下の測定は 0.01 K 程度の精度で行う必要がある。
ここではサーミスターを用いてナフタレン(あるいはビフェニル)の凝固点降下度を求め、溶質の分子量を推定する。
<試薬>
- シクロヘキサン
- ナフタレン
- ビフェニル
VA. サーミスターの電気抵抗の温度変化
サーミスターの電気抵抗 R の温度依存性は、次のアレニウス型の式で表わされる :
\begin{equation}
R(T) = R_0 \exp(B/T)
\label{eq:thermistor}
\end{equation}
ここで T は熱力学温度であり、サーミスターの場合、
一般に指数部の係数の記号には B が用いられ、B 係数と呼ばれる。
たいていのサーミスターの B 係数は およそ 3000 K 程度である。
式 \eqref{eq:thermistor} から
\begin{equation}
\frac{1}{R(T)} \frac{\rmd ~ R(T)}{\rmd~T} = -\frac{B}{T^2}
\label{eq:thermtdev}
\end{equation}
であり、T ≈ 300 Kであれば、
電気抵抗が 10-4 の相対精度で測定できるなら、
温度は 10-4 × T2/B ≈ 0.003 K程度の精度で測定できる。
マルチメータ U1251A の抵抗測定モードの分解能は 50 kΩ レンジで 1 Ω あるので、
今回の測定に十分であると考えられる。
通常のサーミスターは温度を上げると抵抗が小さくなるが(NTC型)、逆に抵抗が大きくなるものなどもある(PTC型)。
操作
- リード線対を約 1 m取ってサーミスターを取り付けマルチメータ U1251A で抵抗値を測定し、
室温付近で 10 kΩ 程度であり、手で温めて抵抗値が下がることを確認する
(先輩たちが作ったものをそのまま使用してよい。断線あるいはショートしていないかを確認する。リード線の抵抗値等は無視してよい)。
- ガラス管の一端を封じ、サーミスターとペン型温度計を入れる。
リード線がペン型温度計に触れてショートしないように注意する。
- ビーカーに水を入れ撹拌しながら、(2) のガラス管を浸して、マルチメータ U1251A を用いて、温度と電気抵抗を測定する。
- ビーカーに氷や熱湯を注いで温度を変え、温度と電気抵抗を測定する。
概ね 0~80 °C の範囲での温度-抵抗挙動を 10~20 °C 間隔で測定すればよい 。
<検討課題>
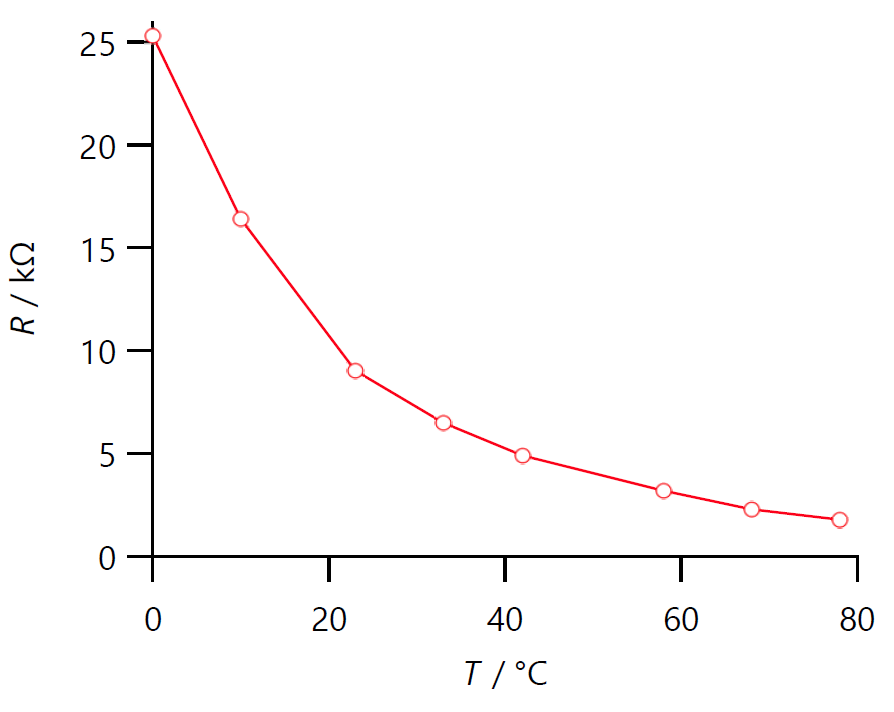
- サーミスターの (i) 温度 T と電気抵抗 R のグラフ、
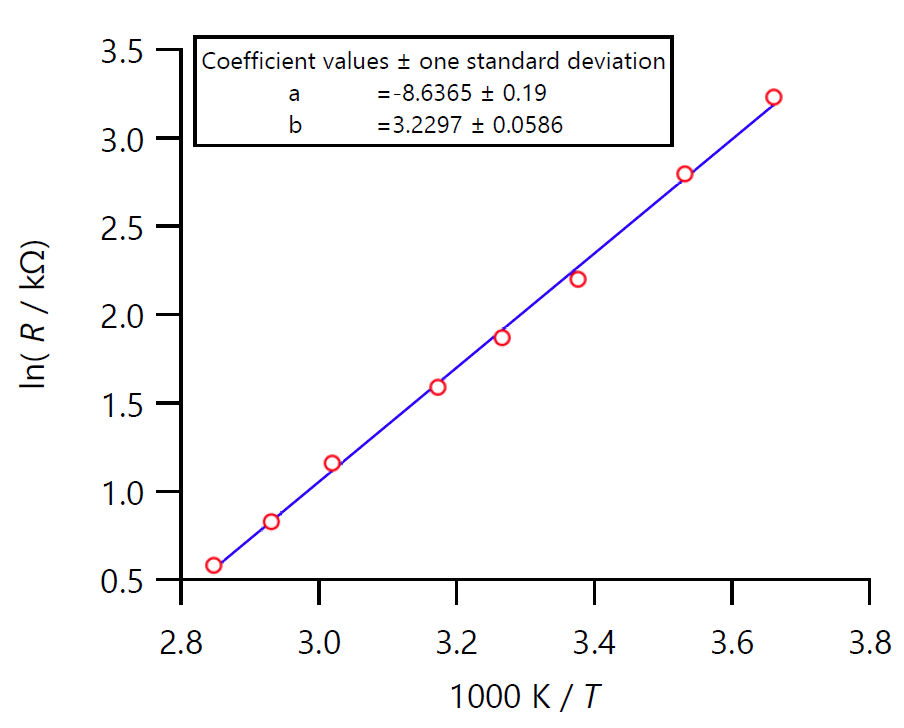
(ii) K/T(あるいは1000 K/T)と ln (R/kΩ) のグラフ(アレニウスプロット)を作成せよ。
- 最小2乗法を適用しサーミスターの B 係数を決定せよ。
実験例
|
|
|
図 V-1a. サーミスターの抵抗 R の温度変化。
|
図 V-1b. サーミスターの B 係数の決定。
|
VB.凝固点降下度による分子量の決定
操作
- 直径 10 mm程度の試験管にシクロヘキサンを 4~5 g 程度、0.01 g まで精確にはかって入れ、撹拌子を入れる。
- シクロヘキサンに浸るようにサーミスターを取り付け、マルチメータ U1251A を用いて抵抗を測定できるようにする。
- PC のデータロガーソフトを立ち上げ、U1251A から5~10 秒おきに抵抗値を読み込むようにセットする。
- あらかじめ作っておいた氷浴に、シクロヘキサンの入った試験管が入る程度の大きさのサンプル管(20 mL程度)を浸す。
- 試験管をサンプル管に差し込み、マグネチックスターラーで撹拌しながら冷却を開始。同時に抵抗値の時間変化の取り込みを開始する。
- シクロヘキサンの凝固が始まり、抵抗値の変化が収まって 10分程度たったら測定を止める。
- 一端試験管を取り出して室温に戻しシクロヘキサンを融解させた後、ナフタレン(あるいはビフェニル)を約 0.1 g 程度 0.1 mg まで精確に秤量して加えて溶解させる。
- 純シクロヘキサンの場合と同様に、シクロヘキサン溶液を冷却して、サーミスターの抵抗値の温度変化をデータロガーで PC に取り込む。
撹拌の際の電磁誘導にともなうノイズを拾うことがあるので、リード線の引き回しに注意する。
マルチメーターの表示が安定しない時は平均値表示機能を利用する手もある。
<検討課題>
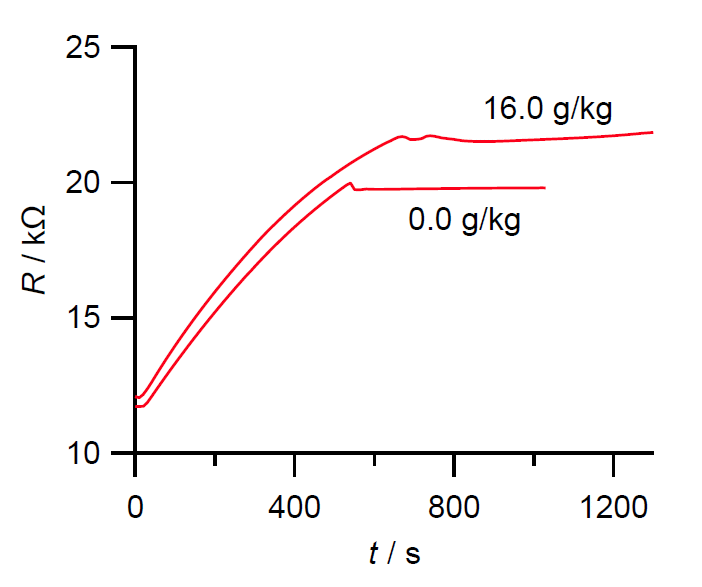
- サーミスターの抵抗の時間変化のグラフを作成せよ。
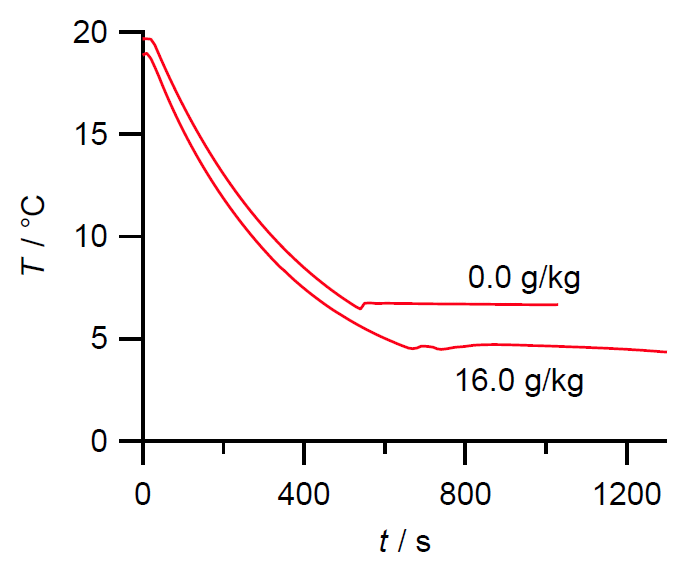
- 先に得た関係式を用いてサーミスターの抵抗値を温度に変換し、
純シクロヘキサンとナフタレン(あるいはビフェニル)のシクロヘキサン溶液の冷却曲線を描き、
凝固点降下度からナフタレン(あるいはビフェニル)の分子量を求める(凝固点降下定数は資料編参照)。
実験例
|
|
|
図 V-2a. ビフェニルのシクロヘキサン溶液の冷却にともなうサーミスターの抵抗変化。
|
図 V-2b. サーミスターの抵抗変化から得られるビフェニルのシクロヘキサン溶液の冷却曲線。
|
凝固点降下の実験のこと
化学教室の学生実験に欠けている重要な要素として、
束一性 colligative properties に関する実験があります。
束一性は、さまざまな物質の間に何か共通の "交換レート" がある、
「物質量 amount-of-substance」が存在することを証拠立てる大事な性質です。
また化学熱力学を実際の問題に適用する上で興味深い対象です。
けれども実際に学生実験の課題として実施する上で、
現在の課題構成の中では、1日で完結することが必要で、
なかなかハードルが高いものがあります。
束一性としては、蒸気圧降下(沸点上昇)、凝固点降下、浸透圧が挙げられますが、
それぞれ定性的に現象に触れる分にはよいのですが、
束一性を示すことを明らかにするには、定量的な測定が求められます。
この点、
凝固点降下の実験が、学生実験に最も適当であると判断しました。
蒸気圧降下(沸点上昇)の実験は、
蒸気を扱う関係で装置がいささか複雑になり、
多数のグループで同時に課題を進行させるのは難しそうでした。
また浸透圧の実験は、(これまた現在の3回生実験の課題構成に欠けている)
高分子やコロイドとの関連で興味のある実験ではあるのですが、
平衡に達するのに時間がかかり、適当な課題を構成するに至りませんでした。
なおこの凝固点降下の実験は、これまでに何回か実施したものの、
いまだ「定番」とはなっていません。
前期の A 実験で実施したこともありましたが、
少し荷が重すぎたようでした。
できれば B3 実験の中に席を作ってやりたいのですが・・・
実験の設計にあたって
凝固点降下で分子量を決めるだけであれば、
有機化学の分野で昔行われたという、
Rast の方法と呼ばれるものがあります。
ぼくはやったことがありませんが、
これはショウノウ campher に有機物を溶かして固化させたのち、
その混合物の融点を測るという手順を踏みます。
ショウノウの融点が 179 °C と高く、物質の溶解度が高くなり有利で、
また凝固点降下定数がおよそ 40 K kg mol-1 と大きいので、
融点の測定精度が 0.1 °C 程度で、十分実用的に分子量測定ができるとのことです
(ショウノウと溶質の質量比は 10:1 程度にとるとのこと)。
実験課題としては、(1) ショウノウ、(2) 標準物質を加えたショウノウ、
(3) 測定試料を加えたショウノウ、の 3 種の融点をはかり、(1) と (2) の融点から融点降下度を決め、
測定試料の分子量を決めるということになるでしょう。
Rast の方法は試料が小量で済み、手軽で、
有機化学実験で使用する融点測定器を利用すれば、
特に装置の問題もありません。
ただこれだけでは、あまりに "花" がなさすぎます。
融点測定器は 6 台あるのですが、
実験グループは 30。
何かの合成実験とでも組み合わせればよいのでしょうが、
ひたすら融点をはかり、
ひたすら装置の空きを待つ実験になりそうでした。
というわけで電気抵抗の温度依存性の実験と抱き合わせて、
高感度の電気抵抗・温度測定の流れの中で、
凝固点降下度を求めるという形に落ち着きました。
サーミスターによる温度測定

|
図 V-3. 実験に使用するサーミスター。
SEMITEC の 103ET-1。下部の黒い粒が感温部。
|
サーミスターは小型で安定なものが多種、安価(~100円)に市販されており、
手軽に利用できます。
ここでは SEMITEC(旧石塚電子)の ET シリーズの 10 kΩ のサーミスター(103ET-1)を使用しました。
103ET-1 の感温部はマッチ棒の頭ぐらいのサイズのビーズ状で、
カタログの値は、25 °Cでの抵抗値が 10 kΩ (± 3 %)で、
B 定数は 3250 K(± 1 %)です。
マルチメータ U1251A は、直流を流した場合の電流と電圧の関係から、オームの法則に従って電気抵抗を評価・表示します 。
マニュアル記載の仕様では、抵抗のレンジが 50 kΩ で 41.2 μA の直流電流を通じることになっています。
ですから U1251A で10 kΩ 程度の抵抗を測定すると、測定に際して 20 μW 程度の発熱が起き、
体温計のように 1/10 K 程度の精度であれば問題ないですが、
1/100 K の測定を目指すなら問題が起きます(熱放散定数が 0.7 mW/K)。
ただし問題にするのが凝固点降下度で、温度差が問題で、また抵抗値がそう大きく変化しないので、
影響はほぼ打ち消されるでしょう。
サーミスターによる温度測定では、この自己発熱の影響が問題になります。
このためカタログ等には、抵抗値として電流値が 0 の場合の値として「ゼロ負荷抵抗値」が記載されています。
なおこれを逆手に取って(?)、自己発熱の熱伝導の変化をモニターし、
サーミスターを湿度センサーや圧力センサーなどとして使用することも行われています。
実験ではサーミスターの温度依存性の測定を行い、
B 係数の決定を行います。
ここでは内径 6 mm ぐらいのガラス管の一端を封じて、
サーミスターとペン型温度計を差し込み、
水浴の中に浸して温度と抵抗値をはかる設定にしています。
ペン型温度計の感温部は先端から 5 mm 程のところにあるので、
サーミスターのビーズがちょうどそのあたりに来るようにセットします。
温度の測定をどのようにするかについては、
熱電対を用いてはかるようにしたこともありましたが、
ペン型温度計を使うのが簡便、確実なようです。
ペン型温度計はセンサーにサーミスターを使用しているので、
醒めた目で見ればサーミスターでサーミスターの温度依存性を調べるという、
いささか茶番じみていますが、
お墨付きのサーミスター(?)で未知のサーミスターをチェックするということで納得してもらいます。
|
|
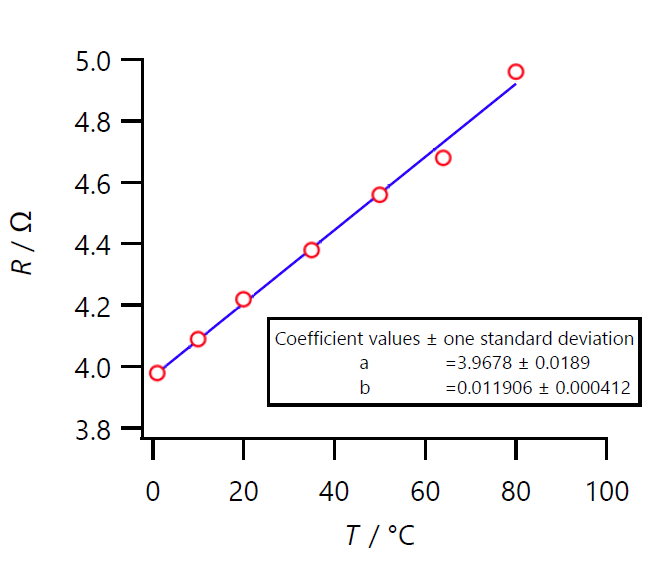
図 V-4. 銅線(L 2 m、φ 0.1 mm)の抵抗の温度変化。
|
学生さんの実験結果を見ると、抵抗値はいささか低めに出るものの(おおむね 1~2 割ほど低い)、
B 係数はだいたいカタログ値程度になっています。
これは温度を下げる方向で実験していて、
十分温度が落ち着いていないうちに測定しているためでしょう
(ペン型温度計の方が温度緩和に時間がかかります)。
また温度範囲は 0~80 °C 程度ということにしていますが、
たまたま寒剤が余っていたので、
学生さんを唆してドライアイスや窒素温度での抵抗をはかってもらったりもしました。
一挙に MΩ 以上の絶縁体になるので、
結構インパクトがあったようです。
こうした測定も、うまく他の課題と調整して組み込みたいところです。
なお時間に余裕があった時には、
金属の温度依存性も調べてもらったこともありました。
講義や教科書で知ってはいても、やったことのない学生が大半で、
実際にはかってみるとサーミスター・半導体との違いが明瞭です。
超伝導の課題で電気抵抗の測定があるのですが、
4 線式の抵抗測定などの前に、こうした素朴な実験をやっておくのは、
よい足慣らしになるかと思います。
図 V-4 に示すのは直径 0.1 mm の銅線を 2 m ほど取って、
抵抗の温度依存性を調べた例です。
これで銅 Cu の抵抗率を計算すると 25 °C で 1.7 × 10-8 Ω m
になり、文献値と一致します。
一方温度係数は 2.8 × 10-3 K-1 で、
文献値 3.9 × 10-3 K-1 より3割がた小さくなっています。
これは使用した銅線の銅の純度等に何か秘密があるのかもしれません。
実験の実際と攪拌の重要性

|
|
図 V-5. 実験風景。
|
学生実験の課題の中で、
スズと鉛の相図の作成の課題で冷却曲線を扱うのですが、
冷却速度は典型的には 1~2 °C/s 程度で、
ここで扱う冷却速度より 100 倍以上速くなっています。
この差が生じるのは、
温度の緩和時間と必要とされる温度の分解能に関わっています。
室温付近で金属の熱伝導度はたいてい 10 W m-1 K-1 以上ありますが、
有機液体の場合はその 1/100 のオーダーです(25 °C のシクロヘキサンは 0.12 W m-1 K-1。
温度拡散係数も 1/100 のオーダー)。
その上、スズと鉛の相図の場合には温度の分解能が 1/10 K 程度ですが、
ここでは 1/100 K 程度までを目指すので、
いよいよ慎重に事を運ばないといけなくなるのです。
昔から凝固点降下の学生実験では行われてきたことですが、
冷却速度を下げるために、
大きめのサンプル管に、試料溶液を入れた試験管を入れ二重にしています。
しかし昔より、溶液量が 5 分の 1 程度になっていることを考えると(体積当たりの表面積が大きくなっている)、
もっと断熱を考慮して、ガラス同士の接触を妨げるように、
紙や綿を詰めた方がいいかもしれません。
特に問題が大きいのは、溶液の攪拌です。
純シクロヘキサンの場合にはまだましですが、
溶液になると結晶が析出してきて粥状態になった時、
濃度の不均一さ(温度の不均一さ)が露わになってきます。
小型の棒状のマグネチック撹拌子を入れて攪拌するようにしているのですが、
結晶粥状態になると攪拌の効率が落ちます。
テフロンのシートの短冊を作って、
「邪魔板」として挿入するとかなり効率は改善されますが、
いっそ手で試験管を振った方がよいようにも見えます。
昔の実験書などには、針金の網やリングを、溶液中で機械的に上下させて攪拌する手法が紹介されています。
このあたりも、まだまだ検討が必要なところです。
さて図 V-2 にシクロヘキサンを溶媒に、ビフェニルの凝固点降下を調べた実験例を示しました
(これはぼくがやった予備実験の結果で、あまり美しくはないですが、
それでも学生諸君よりはましだと自負しています)。
溶液はビフェニル \(m_\mrm{X}\) = 69.4 mg を取って、
シクロヘキサン \(m_\mrm{S}\) = 4.34 g に溶かして調製しました。
凝固点降下度 ΔT は 2.10 °C になり、
シクロヘキサンの凝固点降下度
Ef = 20.8 K kg mol-1
なので、ビフェニルのモル質量は
\[
M = \frac{m_\mrm{X}}{m_\mrm{S}} \frac{E_\mrm{f}}{\Delta T}
= 158~\mbox{g/mol}
\]
となります。
ビフェニル分子式 C12H10 から得られる値は 154.21 g/mol で、
3 % ぐらい大きいですが、まずまずの一致でしょう。
ベックマン温度計のこと

|

|
|
図 V-6a. ベックマン温度計。
左側は凝固点降下用、右側は沸点上昇用。
|
図 V-6b. ベックマン温度計の上部。
右側のベックマン温度計は、長年の使用で少し疲れ気味・・・
|
ご存じの方も多いでしょうが、
凝固点降下の実験には、その昔、
ベックマン温度計を用いた測定が行われてきました。
図 V-6a は研究室に古くから伝わる、ベックマン温度計です。
凝固点降下の実験では、温度が下がる方向で測定するので、
下方向に目盛りが付けられ、
沸点上昇の実験用には、上方向に目盛りが付けられています。
比較的新しい(といってもぼくの学生時代)ベックマン温度計の目盛りつけの範囲は、
0 ~ 5 °C あるいは 0 ~ 6 °C のものが多いようですが、
その昔はここに示すような 0 ~ 4 °C も普通にあったようです。
目盛りは 1/100 °C 刻みで、ルーペで 1/1000 °C まで読みます。
ベックマン温度計を使う実験では、
基準となる温度(純溶媒の凝固点)でだいたい目盛りが 0 になるようにあわせる必要があります。
まずビーカーに温水を取ってベックマン温度計を浸し、
水銀柱が上部の水銀だめ(図 V-6b)の水銀と繋がるようにセットします
(手で温めても OK。前に使った人が温度を上げ過ぎていたりすると、
水銀柱が上部の水銀だめに届かず、ドライヤーで炙ったりする羽目になることもあります)。
次にビーカーの水温を所定の温度より少し高めになるように調整し(シクロヘキサンであれば 7 °C + α)、
ベックマン温度計を浸して温度が落ち着いたところで、
ベックマン温度計をビーカーから取り出して傾け(ひっくり返す人もいます)、
上部の水銀だめのところを、指でパチンと弾いて水銀柱を切り離します。
この切り離すところは手練の技が必要なところで、
ぼくは苦手です。
そうしてベックマン温度計を立てて、
所定の温度で水銀柱の位置が、目盛の 0 付近になっているかチェック。
もし目盛の範囲より高ければ、 0 付近になるまでやり直し。
さらに問題は必要とする溶液量が多いことです。
ベックマン温度計は通常のガラス温度計よりけた違いに多い水銀を用いており、
温度計の感熱部を浸すには 30 mL できれば 50 mL ぐらいの試料溶液が必要になります。
というわけで、ベックマン温度計を使う凝固点降下の実験は、
今や過去の遺物となっています。
特に昨今は水銀を見る目が冷たく険しいものになり、
実験室の倉庫に寂しく眠っているベックマン温度計を見ると、
何か切ない気持ちになるのですが、第2の人生(?)はあるのでしょうか・・・
準備実験のページへ








